メタアナリシスという言葉を耳にしたことはあるものの、「具体的にどのような手法なのか」「システマティックレビューとはどう違うのか」と疑問に感じている方は多いのではないでしょうか。
医学や公衆衛生をはじめとする多くの研究分野において、メタアナリシスは非常に重要な役割を担っています。複数の研究結果を客観的かつ統計的に統合することで、単一の研究では得られない信頼性の高い結論を導き出すことができるからです。
本記事では、メタアナリシスの基本概念や実施するメリット、システマティックレビューとの明確な違いについて分かりやすく解説します。さらに、実際の手順や「フォレストプロット」の見方、「出版バイアス」といった結果を解釈する際の重要な注意点まで網羅的にまとめました。メタアナリシスの全体像を体系的に理解したい方は、ぜひ最後までご覧ください。
メタアナリシスとは?基本概念と目的

メタアナリシスの定義と実施する目的・メリット
結論から言うと、メタアナリシスとは「複数の独立した研究結果を、統計的手法を用いて定量的に統合し、全体的な効果を推定する分析方法」のことです。 過去に行われた類似するテーマの複数の研究データを集め、それらを数学的な手法で一つにまとめ上げることで、より信頼性の高い1つの結論を導き出そうとするのが主な目的です
メタアナリシスを実施する最大のメリットは、個々の研究の限界を補い、真の治療効果や要因の影響をより正確に評価できる点にあります。
例えば、ある新薬の効果を検証した小規模な研究Aと研究Bがあったとします。小規模な研究だけではデータのばらつきが大きく、偶然によって結果が左右されるリスクがあります。
しかし、これらを統合し、サンプルサイズが十分な大規模データとして解析を行うことで、統計的な検出力が高まり、より真実に近い効果量(リスク比やオッズ比など)を導き出すことが可能になります。
つまり、メタアナリシスの目的は、個々の研究のばらつきを克服し、科学的かつ客観的な「最適解」を定量的に示すことにあるのです。
なぜ「エビデンスレベル」が最も高いと言われるのか?
医療や科学の分野では、研究手法によって得られた情報の信頼性を「エビデンスレベル(科学的根拠の強さ)」という階層で評価します。その中で、メタアナリシス(およびシステマティックレビュー)は、エビデンスレベルのピラミッドの頂点、すなわち最も信頼性が高い手法として位置づけられています。
| エビデンスレベル | 内容 |
| レベルI | システマティック・レビューまたはランダム化比較試験のメタアナリシス |
| レベルII | 1つ以上のランダム化比較試験 |
| レベルIII | 非ランダム化比較試験 |
| レベルIVa | コホート研究 |
| レベルIVb | 症例対照研究、横断研究 |
| レベルV | 症例報告、ケースシリーズ |
| レベルVI | 専門委員会や専門家個人の意見 |
その理由は、単一の研究結果や研究者の主観によるバイアス(偏り)を極限まで排除できる手法だからです。
質の高い研究手法とされるランダム化比較試験(RCT)であっても、対象となった特定の集団や設定された条件に結果が依存してしまう可能性があります。
しかし、メタアナリシスでは、世界中で行われた複数の研究データを網羅的に集め、客観的な統計手法を用いて統合します。さらに、各研究の精度(サンプルサイズの大きさや標準誤差の小ささなど)に応じて適切な重みづけを行い、信頼性の高い研究結果ほど最終的な結論に大きく貢献するように計算されます。
様々な環境や集団で行われた複数の研究を厳密に統合することで、単一の研究では証明しきれなかった普遍的な事実(一般化可能性の高い結果)を提示できるため、メタアナリシスはエビデンスレベルが最も高いと評価されているのです。
>>エビデンスレベル(科学的根拠の強さ)のピラミッドや各研究デザインの信頼性について、さらに詳しく知りたい方はこちらの記事もご覧ください。
システマティックレビューとの違いと国際的なガイドライン
システマティックレビュー(SR)とは?
メタアナリシスと頻繁に混同されるのが「システマティックレビュー(Systematic Review: SR)」です。
システマティックレビューとは、特定のテーマ(リサーチクエスチョン)に関する既存の研究を、系統的かつ網羅的に収集・評価・統合する「包括的な文献レビュー手法」を指します。 あらかじめ定められた厳密な検索手順に従って世界中のデータベースから論文を検索し、研究の質(バイアスのリスクなど)を批判的に吟味した上で、得られた知見を整理します。システマティックレビューの特徴は、結果の統合が「定性的」であっても「定量的」であってもよい点にあります。つまり、データを数値でまとめられない場合でも、文章や表を用いて全体的な傾向を論理的にまとめることが可能なのです。
メタアナリシスとシステマティックレビューの決定的な違い
システマティックレビューとメタアナリシスの決定的な違いは、「統計的手法を用いて定量的な統合を行っているかどうか」にあります。
システマティックレビューが文献の系統的な収集と評価(定性的・定量的の両方を含む)という大きな枠組みであるのに対し、メタアナリシスは、常に定量的な評価を実施し、主に統計的手法による結果の統合に焦点を当てた分析方法を指します。
言い換えれば、メタアナリシスはシステマティックレビューのプロセスの中に含まれる「解析手法の一つ」です。
システマティックレビューの中で、複数の研究結果(効果量)が類似した指標で測定されており、統計的にまとめることが可能かつ適切であると判断された場合にのみ、メタアナリシスが実行されます。
したがって、「システマティックレビューは行ったが、メタアナリシスは行わなかった」という論文は存在しますが、メタアナリシスを行うためには、その前提として必ずシステマティックレビューによる網羅的な文献収集が行われていなければなりません。
報告の質を担保するガイドライン「PRISMA声明」とは
システマティックレビューやメタアナリシスはエビデンスレベルが高いとされていますが、その質を担保するためには、研究プロセスが透明であり、客観的に評価可能でなければなりません。
そこで重要になるのが「PRISMA声明」です。
PRISMA声明とは、システマティックレビューやメタアナリシスを報告する際に遵守すべき国際的なガイドラインです。
研究者はPRISMA声明に従い、「どのようなデータベースを、どのような検索式で検索したのか」「どのような基準で論文を採択・除外したのか」といった使用した方法論や選択基準を論文内に明確に記述する必要があります。
これにより、他の研究者が同じ手順を再現し、結果の妥当性を検証することが可能になります。 現在、質の高い医学雑誌の多くは、メタアナリシスの論文投稿においてこのPRISMA声明の遵守を必須条件としています。
メタアナリシスのやり方・手順
1. 研究課題の設定と文献の網羅的な収集・選択
メタアナリシスのやり方は、大きく分けて「事前の文献収集」と「統計解析」のフェーズに分かれます。
最初のステップは、明確な研究課題(リサーチクエスチョン)の設定です。
一般的には「PICO(Patient:対象患者、Intervention:介入、Comparison:比較対照、Outcome:結果)」というフレームワークを用いて検証したいテーマを具体化します。
次に、この設定に基づいて検索式を作成し、PubMedなどの主要なデータベースから関連する文献を網羅的に収集します。
その後、あらかじめ定めた包含基準と除外基準に沿って、タイトルや抄録のスクリーニング、さらには本文の精読を行い、最終的にメタアナリシスに組み込む研究を厳選します。
2. データの抽出と統計学的な統合(解析)
対象となる研究が選定されたら、各論文から必要なデータ(サンプルサイズ、イベント発生数、平均値など)を抽出します。そして、抽出したデータを用いて統計学的な統合を行います。
データの統合には、各研究の「効果量(オッズ比、リスク比など)」と「精度の指標」を用いて、それらを統合した全体効果量を算出します。
このとき、各研究結果のばらつき(異質性)を考慮して統計モデルを選択します。各研究が全く同じ母集団から抽出されたと仮定する「固定効果モデル」と、研究ごとに結果が大きく異なっていることを前提とし、そのばらつきを許容する「変量効果モデル」があります。
医療分野のように、研究が行われた環境や患者の背景が微妙に異なる場合は、より柔軟な「変量効果モデル」が採用されることが多くなっています。
>>無料の統計ソフト『EZR』を使って実際にメタアナリシスを行う手順や、データセットの作り方については、こちらの記事で詳しく解説しています。
メタアナリシスの結果の見方と重要な注意点
結果を視覚化する「フォレストプロット」の見方
メタアナリシスの結果は、「フォレストプロット」と呼ばれる特徴的なグラフを用いて視覚的に提示されます。論文を読む際は、このグラフの見方を理解しておくことが必須です。
フォレストプロットでは、縦軸に統合した各研究の名前が並び、横軸に効果量(オッズ比やリスク比など)が示されます。下記がフォレストプロットの一例です。
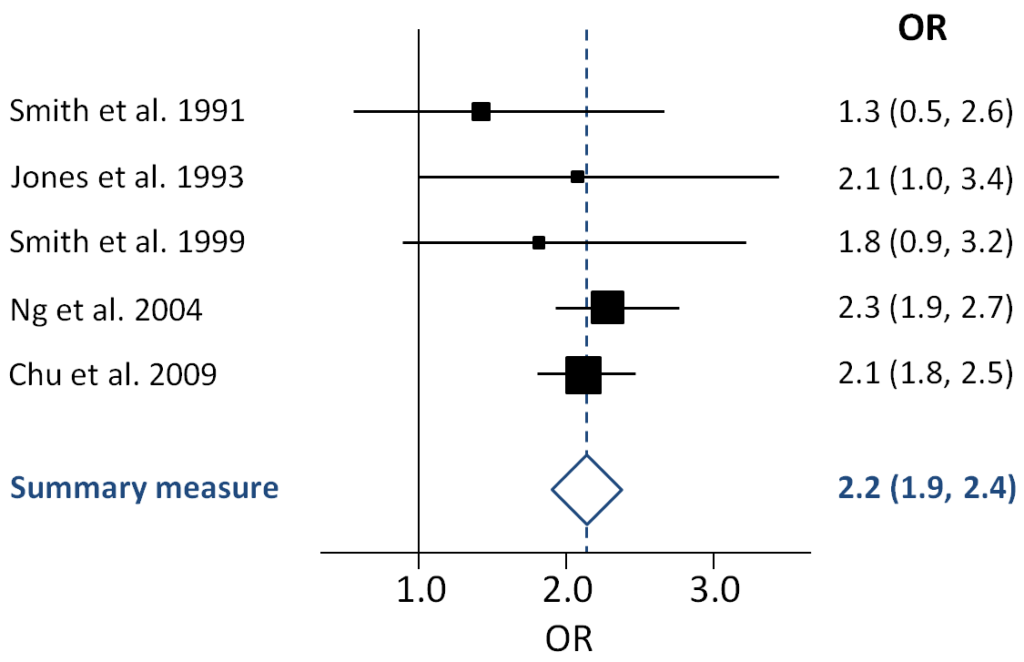
各研究の結果は、四角い「箱」とそこから伸びる「横線」で描かれます。箱の位置がその研究の効果量の点推定値を示し、箱の大きさがその研究の重みを表します。横線は95%信頼区間を示しています。
そして、プロットの一番下にある「ひし形」が、全研究を統合した最終的な効果量(メタアナリシスの結果)です。このひし形が、効果がないことを示す基準線(リスク比やオッズ比なら「1」、平均値の差なら「0」の縦線)と交わっていなければ、「統計的に有意な差がある」と判断することができます。
結果を歪めるリスク「出版バイアス」とは
メタアナリシスの結果を解釈する上で、最も警戒すべき落とし穴が「出版バイアス」です。
出版バイアスとは、「統計的に有意な結果や肯定的な結果が出た研究の方が、そうでない研究(有意差なし、否定的な結果)よりも学術雑誌に掲載(出版)されやすい傾向」のことです。
仮に、新薬の効果がないことを示す研究が存在していても、それらが出版されずにお蔵入りになっていれば、メタアナリシスを行う際に入手可能な論文は「効果があった」とするものばかりに偏ってしまいます。
その結果、統合された効果量が実際の効果よりも過大評価される方向に歪んでしまう危険性があるのです。
出版バイアスの有無を視覚的に調べるためには、「ファンネルプロット」というグラフが用いられます。
これは縦軸に研究の精度(サンプルサイズなど)、横軸に効果量をとった散布図で、出版バイアスがなければ点は逆さまの漏斗(ファンネル)のように左右対称に分布すると期待されます。
非対称な分布が見られる場合は出版バイアスの存在が疑われ、Egger検定などの統計手法を用いてさらに定量的に評価が行われます。
>>出版バイアスが起きてしまう原因や、ファンネルプロットを用いた具体的な評価方法については、こちらの記事で分かりやすくまとめています。
研究間のばらつきを示す「異質性」への配慮
最後に確認すべき重要なポイントが「異質性」です。
異質性とは、統合の対象となったそれぞれの研究で得られた効果の大きさが、研究間でどれくらい「ばらついているか」「異なっているか」の度合いを示しています。
研究のデザインや対象患者の背景などが研究ごとに異なると、結果にも大きなばらつきが生じます。異質性は主に「I^2(アイ二乗)統計量」という指標で評価され、一般的に25%以下なら異質性が低く、25〜50%で中等度、50〜75%で高度、75%以上で極めて高度な異質性があると判断されます。
もし高度な異質性が見られる場合、そもそもそれらの研究を一つに統合すること自体が適切でなかった可能性や、結果の解釈を慎重に行う必要性が生じます。
まとめ
メタアナリシスは、複数の研究結果を統計的に統合し、科学的に最も信頼性の高いエビデンスを提供する強力なツールです。システマティックレビューによる厳密な文献収集を基盤とし、PRISMA声明などのガイドラインを遵守することで、その質と透明性が担保されます。
一方で、フォレストプロットによる正しい結果の解釈や、出版バイアス、異質性といった限界や注意点を理解しておくことも欠かせません。本記事で解説した基本概念や手順、結果の見方を身につけることで、専門的な医学論文や研究データをより深く、正確に読み解くことができるようになるでしょう。











コメント